کاربرد اسید در مواد منفجره
باروت سیاه
باروت سیاه که به باروت نیز معروف است به احتمال زیاد اولین ترکیب مواد منفجره بوده است. ۲۲۰ سال پیش از میلاد انفجار باروت سیاه گزارش شده است. چند شیمیدان چینی در موقع جدا کردن طلاه از نقره طی یک واکنش شیمیایی در دمای پایین، باروت سیاه را به طور تصادفی ساخته بودند. آن ها پتاسیم نیترات(KNO3) [که با نام سالت پتر شناخته شده است] و گوگرد را به سنگ معدن طلا در کوره شیمیایی اضافه کردند ولی افزایش ذغال را در مرحله اول واکنش فراموش کردند. آنها برای رفع اشتباه خود، ذغال را در مرحله نهایی اضافه کردند. آن ها نمی دانستند باروت سیاه را کشف کردند که منجر به انفجار مهیبی شد.
باروت سیاه حاوی یک سوخت و یک اکسنده است. سوخت یک مخلوط پودری از ذغال سنگ و گوگرد است که با پتاسیم نیترات (اکسنده) مخلوط میشود. فرایند اختلاط در سال ۱۴۲۵ هنگامی که فرایند ریز کردن ذرات یا دانهبندی توسعه پیدا کرده بود فوقالعاده پیشرفت کرد. از چرخهای سنگین برای آسیاب کردن و پرس سوختها و اکسندهها به صورت یک توده جامد که متعاقبا به دانههای کوچکتری تبدیل میشوند استفاده شد. این دانه ها حاوی مخلوط یکنواختی از سوخت و اکسنده است در نتیجه باروت سیاهی بدست میآید که از نظر فیزیکی و انفجار برتری دارد. باروت ریزشده به تدریج در اسلحههای کوچک و نارنجکهای دستی در طول قرن ۱۵ و اسلحههای کوچک و نارنجک های دستی در طول قرن ۱۵ و اسلحههای بزرگ در قرن ۱۶ مورد استفاده قرار گرفت.
اولین یادداشتهای استفاده از باروت سیاه در مهندسی عمران مربوط به سالهای ۱۵۷۲-۱۶۴۸ برای لایروبی رودخانه نیمن در اروپای شمالی و در سال ۱۶۲۷ برای بازیابی معادن مجارستان به عنوان کمک انفجار بوده است. به زودی از باروت سیاه به منظور انفجار در آلمان، سوئد، و سایر کشورها استفاده شد. استفاده از باروت سیاه به منظور انفجار در انگلستان برای اولین بار در سال ۱۶۷۰ در معادن مس کرنیش صورت گرفت. صنایع بوفورس در سوئد در ۱۶۴۶ تولید کننده عمده باروت تجارتی در اروپا بود.
نیتروگلیسیرین
در قرن ۱۹ محدودیتهای باروت سیاه به عنوان یک ماده منفجره، اشکار شده بود عملیات سخت معدنکاری و تونل کاری نیاز به یک ماده منفجره بهتری داشت. در ۱۸۴۶ اسکانیو سوبررو پرفسور ایتالیایی نیتروگلیسیرین مایع (C3H3O5(NO3)3) را کشف کرد. او به زودی به ماهیت انفجاری این ماده پی برد و تحقیقات خود را ادامه نداد. چند سال بعد مخترع سوئدی به نام امانوئل نوبل فرایندی برای تولید نیتروگلیسیرین پیدا کرد و در سال ۱۸۶۳ با فرزندش آلفرد، کارخانه تولید کوچکی در هلنبرگ نزدیک استکهلم تاسیس کرد. روش تولید اولیه آنها، اختلاط گلیسرول با مخلوط سرد اسید سولفوریک و نیتریک اسید در یک پارچ سنگی بود. این مخلوط به صورت دستی همزده شد و با و با آب یخ سرد نگه داشته میشد. پس از کامل شدن واکنش، مخلوط درون مقدار زیادی آب ریخته میشد. دومین فرایند تولیدی، ریختن گلیسرول و مخلوط سردشده اسیدها به درون ظرف سربی مخروطی شکل با سوراخ های به هم فشرده بود. محصول نیتروگلیسیرین از میان این محدودیتها به درون حمام آب سرد جریان داشت. هر دو روش شامل شستن نیتروگیلیسیرین با آب گرم و یک محلول قلیایی گرم برای حذف اسیدها بودند. نوبل اقدام به دریافت مجوز تاسیس کارخانه نیترگلیسیرین کرد. این کارخانهها معمولا بسیار نزدیک به محل مصرف آنها ساخته میشدند. زیرا در حمل نیتروگلیسیرین مایع احتمال تخریب عمارات و مرگ انسانها وجود داشت.
نیتروگلیسیرین نسبت به باروت مزیت زیادی دارد. زیرا مولکول آن هر دو جز سوخت و اکسنده را دارد. این خاصیت بیشترین حد تماس برای هر دو جز تشکیل دهنده یک ماده منفجره را فراهم میکند. نیتروگلیسیرین یک ماده منفجره ثانویه بسیار قوی با اثرات تخریبی بالاست و یکی از برترین و پراستفادهترین اجزای ترکیبی برای مواد منفجره تجاری ژلاتینی است.
نیتروگلیسیرین همچنین یک منبع انرژی بالا را در پیشرانهها را فراهم میکند و در ترکیب با نیتروسلولز و تثبیتکنندهها، جز اصلی پودرهای انفجاری و پیشرانههای جامد موشکی است. نیتروگلیسیرین سمی است و سر و کار داشتن با آن موجب سردرد میشود و در اثر انفجار محصولات سمی تولید میکند. نیتروگلیسیرین در آب نامحلول اما در بیشتر حلالهای آلی و تعداد زیادی از ترکیبات نیتروآروماتیک محلول و با نیتروسلولز تشکیل ژل میدهد. محلول عاری از اسید آن خیلی پایدار است. اما نسبت به ضربه فوقالعاده حساس است. برخی از خواص نیتروگلیسیرین در جدول زیر آمده است.
خواص نیتروگلیسیرین
|
مشخصات |
دادهها |
| رنگ | زرد روغنی |
| وزن مولکولی | ۱/۲۲۷ |
| نقطه ذوب(°C) | ۱۳۰ |
| دمای اشتعال حرارتی(°C) | ۲۰۰ |
| چگالی در °C 20 (g/cm3) | ۵۹/۱ |
| انرژی تشکیل(KJ/kg) | ۱۵۴۷- |
| آنتالپی تشکیل(KJ/kg) | ۱۶۳۳- |
نیتراسیون
نیتراسیون نقش مهمی در تولید مواد منفجره بازی میکند. مثلا اکثر مواد منفجره نظامی و تجاری که معمولا مورد استفاده قرار میگیرند، مانند TNT، RDX، نیتروگلیسیرین، PETN و غیره همگی از روش نیتراسیون تولید میشوند. نیتراسیون یک واکنش شیمیایی است که به وسیله آن گروههای نیترو (NO2) وارد ترکیبات آلی میشود. این واکنش یک جانشینی یا تبادل دوتایی است که یک یا دو گروه نیترو از عامل نیتره کننده، جانشین یک یا چند گروه(معمولا اتمهای هیدروژن) از ماده نیتره شونده میشوند.
نیتروگلیسیرین از تزریق گلیسیرین خیلی غلیظ به داخل محلول خیلی غلیظ به داخل محلول خیلی غلیظ اسید نیتریک و اسید سولفوریک در دمای کنترل شده تهیه میشود.
مخلوطها به طور پیوسته هم زده میشوند و با برین(brine) خنک میشوند. در انتهای واکنش، نیتروگلیسیرین و اسیدها به داخل یک جداکننده ریخته میشوند. که بلافاصله نیتروگلیسیرین در اثر نیروی ثقل جدا میشود. به منظور حذف هرگونه اسید باقیمانده، نیتروگلیسیرین با آب و کربنات سدیم شسته میشود. برای پرهیز از ذخیره حجمی مواد خطرناک، محصول شسته شده بلافاصله فرایند بعدی را طی میکند. فرایند تولید نیتروگلیسیرین میتواند به صورت یک فرایند پیوسته با وارد کردن خوراک مخلوط اسیدهای تازه به داخل محفظه واکنش و خروج نیتروگلیسیرین و اسیدهای استفاده شده صورت گیرد. در این روش نیتروگلیسیرین با بازده بالا همراه با مقدار کمی محصول جانبی تولید میشود. واکنش شیمیایی تولید نیترگلیسیرین در واکنش زیر نشان داده شده است.
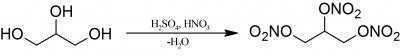
حمل و نقل نیتروگلیسیرین و استرهای مشابه خیلی خطرناک است و فقط به صورت محلول در حلالهای غیرمنفجره یا مخلوط با مواد بیاثر خیلی پودر شده که حاوی بیش از ۰٫۵ درصد نیتروگلیسیرین نباشد حمل میشود.
امروزه از نیتروگلیسیرین در مواد منفجره نظامی استفاده نمیشود و از آن فقط در پیشرانهها و مواد منفجره تجاری استفاده میشود. به خاطر مایع بودن آن در دمای محیط به آسانی داخل مظروفش ریخته میشود. هر چند وقتی از آن به عنوان پیشرانه استفاده میشود از عملکرد بالستیکی نامنظم لطمه میبیند. این به خاطر آن است که وقتی پوسته میچرخد مایع شروع به جابجایی میکند. نیتروگلیسیرین همچنین خیلی حساس است و به راحتی میتواند آغاز شود. بنابراین همیشه بوسیله جذب آن به داخل کیزلگور برای بدست آوردن دینامیت یا ژلاتینی کردن آن با نیتروسلولز برای تولید ژلهای انفجاری، غیرحساس میشود.
