بازیابی اسید سولفوریک
اسید سولفوریک در بسیاری از فرآیندها به عنوان کاتالیزگر مورد استفاده قرار میگیرد. بر این اساس پژوهشگران پیوسته در جستجوی روشهای موثر بازیابی اسید سولفوریک هستند. در برخی موارد برای این مظور اسید مورد استفاده تصفیه یا تمیز میشود و مورد استفاده مجدد قرار میگیرد. اما در مواردی که چنین عملی مورد نظر نباشد اسید سولفوریک قابل بازیابی، پس از تجزیه شیمیایی، به عنوان خوراک برای ساخت مجدد اسید سولفوریک مورد استفاده قرار میگیرد. در ادامه درباره این دو فرآیند توضیح میدهیم.
روشهای بازیابی سولفوریک اسید
اسید سولفوریک و نمکهای سولفات، که پیش از این به عنوان دورریز معرفی شدند، ماده اولیه بسیار خوبی برای تولید گوگرد دیاکسید به منظور تولید مجدد اسید سولفوریک هستند. چنانکه گفتیم اسید سولفوریک در برخی فرآیندها مانند آبگیری و یا آماده سازی سطوح فلزات برای آبکاری، به عنوان کاتالیزگز مورداستفاده قرار میگیرد. این اسید ممکن است برای بازیابی نخست تصفیه و سپس تغلیظ شود و یا ممکن است با روشهای شیمیایی تجزیه شده و دوباره از محصول آن (SO2) برای تولید اسید سولفوریک استفاده گردد.
۱- فرآیند بازیابی و تغلیظ: اگر اسید سولفوریک به مواد آلی آغشته باشد میتوان آن را به روش زیر بازیابی کرد:
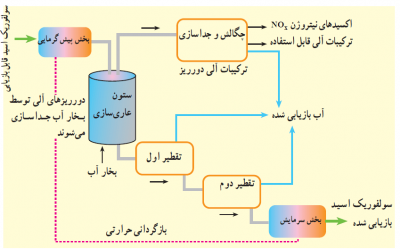 شکل۱: فرآیند بازیابی و تغلیظ اسید سولفوریک
شکل۱: فرآیند بازیابی و تغلیظ اسید سولفوریک
نخست اسید را حرارت میدهند و آن را به برج عاریسازی (Stripping) میفرستند تا با استفاده از بخار آب، مواد آلی آن زدوده شود. آنگاه اسید را با روش تقطیر تغلیظ میکنند. مزیتهای این روش به شرح زیر است:
- انرژی گرمایی حاصل از تشکیل اسید سولفوریک (در مرجله نهایی) برای مرحله اول گرم کردن، در فرآیند بازیابی اسید مورد استفاده قرار میگیرد.
- جابجایی مایعات در این فرآیند عمدتا تحت تاثیر نیروی ثقل آنها انجام میشود در نتیجه نیازی به صرف هزینههای گزاف برای تامین برق و خرید پمپهای ضد اسید برای جاری ساختن مایعات در لولهها نیست. در این فرآیند ظرفهای واکنش باید ضد اسید باشند لذا بیشتر از ظروف شیشه ای و تفلون استفاده میکنند.
تغلیظ اسیدسولفوریک بازیابیشونده برای جداسازی آب و کاهش حجم انجام میگیرد. با این کار نه تنها در مرحله بعد به کورهای با حجم کمتر نیاز است بلکه انرژی مصرفی نیز کاهش مییابد. میزان تغلیط اسید بازیابی شونده نیز به ناخالصیهای موجود در آن بستگی دارد. به این ترتیب تغلیظ در نقطهای متوقف میشود که این ناخالصیها شروع به جداشدن از اسید میکنند.
۲- فرآیند مولکول شکنی(Cracking) در فرآیند بازیافت: در این فرآیند پس از مرحله تغلیظ، اسید با هوای فشرده مخلوط شده و در کورهای با دمای ۱۰۰۰ تا ۱۲۰۰ درجه سانتیگراد تجزیه میشود.
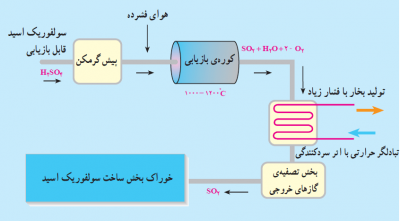
شکل۲: بازیابی اسید سولفوریک در فرآیند مولکول شکنی
معادله واکنش به صورت زیر است:
H2SO4→ SO2 + H2O + 1/2 O2
گاز گاز گاز مایع
در این فرآیند بهترین نتیجه در شرایطی حاصل میشود که زمان قرارگرفتن نمونه در کوره ۳ ثانیه باشد. تامین گرما برای این فرآیند گرماگیر است می توان از منابع انرژی در مجتمع شیمیایی استفاده کرد تا تقاضا برای مصرف انرژی کاهش یابد.
